|
Chémia a elektrina
Chemické reakcie sú vždy spojené s výmenou elektrónov. Elektróny
ako nositelia záporného náboja tvoria elektrický prúd. Preto určité
vhodné chemické reakcie môžeme využiť ako zdroj elektriny. Na
princípe premeny chemickej energie na elektrickú pracujú galvanické
články a batérie (tužkové baterky, štvorcové baterky, autobatérie).
Elektrický prúd naopak môže vyvolať chemické zmeny v roztokoch a
taveninách látok. Elektrického prúdu sa využíva pri elektrolýze, galvanickom pokovovaní, elektroforéze, elektroanalýze, výrobe monočlánkov a batérií a inde.
Obr.
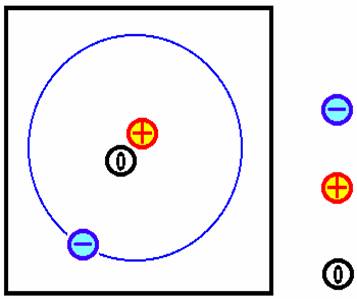
Model atómu -
elektrón, častica so záporným nábojom -
protón, častica s kladným nábojom
Atóm je častica zložená z jadra a obalu. Obal tvoria elektróny (u
vodíka jeden elektrón), ktoré vedú elektrický prúd v kovoch. Ak
stratí atóm jeden alebo viac elektrónov, začne prevládať kladný náboj
jadra a vzniká kladne nabitá častica - katión. Ak získa atóm jeden alebo viac elektrónov, vzniká záporne nabitá častica - anión. Katióny a anióny vedú elektrický prúd v roztokoch a taveninách elektrolytov. Neutróny sú častice bez náboja a na vodivosti sa nezúčastňujú.
Laclancheov
galvanický článok
Obr.
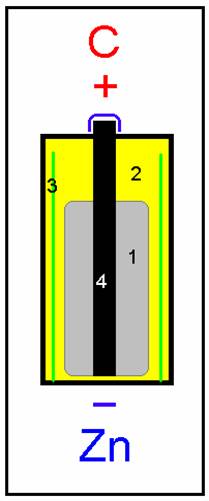
Laclancheov článok 2
– salmiak (cklorid amónny) 3
– elektróda zo zinku 4
– elektróda z uhlíku
Laclancheov článok je najpoužívanejším chemickým zdrojom
elektrickej energie. Napätie článku je 1,5 V. Tri takéto články
tvoria známu štvorcovú batériu s napätím 4,5V.
Ak zapojíme článok do elektrického
obvodu prebiehajú elektrochemické procesy, ktoré spôsobujú vznik
elektrického prúdu a postupné vyčerpávanie článku. Zápornú elektródu článku tvorí dutý zinkový valec, kladnú elekródu uhlíkový kolík, ako elektrolyt slúži chlorid amónny. Burel je depolarizátor (predlžuje životnosť článku). Pri konštrukcii starších typov článkov sa často používali aj ťažké kovy (Ni, Cd). Tieto predlžovali životnosť a zlepšovali niektoré vlastnosti článku. Ťažké kovy sú však toxické, poškodzujú prírodu a zdravie človeka, preto sa od ich využitia upúšťa. |
Pokus
Elektrolýza NaCl
V nádobe s objemom asi 0,5 l priprav roztok kuchynskej soli vo
vode. Roztok dôkladne premiešaj, aby sa všetka soľ rozpustila. Uhlíkové
(železné, medené) elektródy upevni do stojana (stojan zhotovíme
tak, že ceruzku, alebo drôt zapichneme do plastelíny). Elektródy
spoj vodivo s 9 V batériou, do obvodu zapoj dve bicyklové žiarovky.
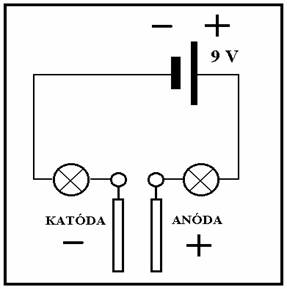
Obr. Schéma elektrického obvodu využitého pri elektrolýze NaCl -
zdroj 9 V -
dve žiarovky -
vodiče - dve elektródy (katóda je elektróda so záporným nábojom, lebo priťahuje katióny - častice s kladným nábojom)
Žiarovky v elektrickom obvode svietia, čo je dôkazom prechodu
elektrického prúdu roztokom elektrolytu. Pri elektródach sa uvoľňujú
plyny - vodík na katóde a chlór na anóde. Pri katóde vzniká
hydroxid sodný a pri anóde kyselina chlorovodíková. Chemické
reakcie Elektrolýza NaCl K(-)
Na+ + H2O
===> NaOH + H+
H+ +
1e-
===> H
2H
===> H2
A(+)
Cl-
- 1e-
===> Cl
2Cl
===> Cl2
Cl2 +
H2O
===> HCl + HClO
Kyselina a hydroxid sa dajú dokázať farebným indikátorom, vodík skúškou horenia. Priestor medzi dvoma elektródami sa dá oddeliť škrupinou vajca. Škrupina slúži ako polopriepustná membrána - diafragma, bráni miešaniu produktov elektrolýzy, nebráni však prechodu elektrického prúdu (prechodu aniónov).
Pokus
Citrón ako zdroj prúdu
Na pokus potrebuješ čerstvý citrón, zariadenie na meranie
elektrického napätia (voltmeter), medený a oceľový drôtik. Drôty
z mede a ocele slúžia ako elektródy, elektrolytom je šťava
citróna obsahujúca vodu, kyselinu citrónovú a iné látky. Drôty
zapichni do citróna a napoj ich na voltmeter, sleduj výchylku
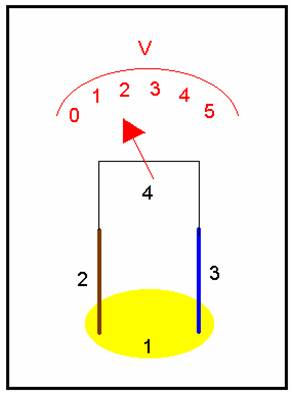
Obr.
Monočlánok z citrónu 1-citrón 2-medená
elektróda 3-oceľová
elektróda 4-voltmeter |